
Kimyasal Tepkimelerde Hız (5) YouTube
Tepkime Hızları İçindekiler [ göster] " Tepkime hızları ", tepkimelerin başladıktan sonraki hızları ile ilgili bir kavramdır. Bazı tepkimeler çok hızlı gerçekleşirken, bazıları çok yavaştır. Hava yastıklarının açılması veya bombaların patlaması gibi bazı kimyasal tepkimeler başladıkları anda biterler.

KİMYASAL TEPKİMELERDE HIZ 3.bölüm, Hız Bağıntısı, Kademeli tepkimelerde Hız 11. Sınıf Kimya
1. Basınç-Hacim 2. Renk 3. İletkenlik gibi fiziksel özelliklerin değişimi tepkimenin gidişatı hakkında bilgi verir. ÖRNEK: Hem basınç hem de hacim artış veya azalmasıyla tepki- me hızı izlenebilir. Mg + 2HCl (suda) Æ MgCl2 (suda) + H2 (g) (Gaz çıkışı) N2 (g) + 3H2 (g) Æ 2NH3 (g) (Basınç azalması) C2H4 (g) + Br2 (suda) Æ C2H4Br2 (g) (Renk takibi)

Tepkime Hızı Ölçülmesi Kimya Ayt Konu Anlatımı
Denklemi n A + m B → p P + q Q şeklinde olan tek basamaklı bir kimyasal tepkime için hız eşitliği aşağıdaki gibi yazılır. Burada k hız sabitidir. Hız denklemi yazılırken sadece gaz ve çözelti ( aqua) halindeki girenler yazılır. Çünkü katı ve sıvıların molariteleri sabittir. Çok basamaklı tepkimeler

AYT Kimya 11. Sınıf Ders İşleyiş Modülleri Modül6 Kimyasal Tepkimelerde Hız Nesibe Aydın
KİMYASAL TEPKİMELERDE HIZ KONU ANLATIMI - Yepyeni - Müfredata uygun - Anlaşılır - Pratik - Akılda kalıcı - KİMYA BİLMEK İSTEYENLERİN TERCİHİ :)KİMYASAL TEPKİ.

KİMYASAL TEPKİMELERDE HIZ1 Ortalama Hız Hız Takibi Yöntemleri Konu Anlatımı Soru Çözümü11.Sınıf
Kimyasal Denge. Kimyasal denge, iki yönlü bir tepkimede ürünlerin meydana geliş hızının, ürünlerden tekrar tepkimeye girenlerin meydana geliş hızına eşit olduğu durumdur. Böyle denklemlerde tepkimenin her iki tarafa olabileceğini göstermek için çift yönlü ok" ↔" kullanılır. Genel olarak şöyle göstermek mümkündür:

Kimyasal Tepkimelerde Hız Bölüm 3 YouTube
Kimyasal reaksiyonların hızlarını ölçen, mekanizmalarını inceleyen kimya dalına. kimyasal kinetik denir. 1.1. Tepkime Hızlarının İncelenmesi. A (g) + B (g) → C (g) + D (g) gibi kimyasal tepkimelerde, tepkime süresince girenlerin miktarı azalırken ürünlerin miktarı artar. Bu artma ve azalma ne kadar hızlı oluyorsa tepkime.

Kimyasal Tepkimelerde Denge Ünitesi Kimya
Kimyasal tepkimelerde hız ifade edilirken madde miktarındaki değişim genelde mol veya molarite ile ifade edilir. Kimyasal tepkimelerde hız tepkimeye giren maddelerin özelliklerindeki değişimler izlenerek ölçülebilir. Örneğin renk, basınç, hacim, iletkenlik gibi değerlerdeki değişimlerden hız ölçülebilir. 1. Çarpışma Teorisi

Kimyasal tepkimelerde hız DonanımHaber Forum
11.Sınıf Kimya 6. Ünite Kimyasal Tepkimelerde Denge Ders Notları-Test Soruları Ve Cevapları. 11.Sınıf Kimya Kimyasal Tepkimelerde Enerji Konu Anlatımı Ve Sorular. 11.Sınıf Kimya Kimyasal Tepkimelerde Elektrik Konu Anlatımı Ve Sorular. 11.Sınıf Kimya Kimyasal Tepkimelerde Denge Konu Anlatımı Sorular Ve Cevaplar.

Tepkime Hızı (Kimya) YouTube
Kimyasal Tepkimelerde Hız > Tepkime Hızları. Kimyasal bir tepkimenin hızı, tepkimeye giren madde ya da ürünün konsantrasyonunun (derişimi) değişim hızının, eşitlenmiş denklemdeki katsayısına bölümü olarak tanımlanmıştır. Tepkimeye giren maddelerin değişim hızı için negatif.

Kimya AYT Kimyasal Tepkimelerde Hız6 YouTube
KİMYASAL TEPKİMELERDE HIZ KONU ANLATIMI - Yepyeni - Müfredata uygun - Anlaşılır - Pratik - Akılda kalıcı - KİMYA BİLMEK İSTEYENLERİN TERCİHİ :)KİMYASAL TEPKİ.

AYT Kimya 11. Sınıf Ders İşleyiş Modülleri Modül6 Kimyasal Tepkimelerde Hız Nesibe Aydın
Orbital Yayınları

Kimyasal Tepkimelerde Hız 3 YouTube
Kimyasal Tepkimelerde Hız, Endotermik Tepkimeler, Ekzotermik Tepkimeler, Hız Tayini, Çarpışma Kuramı, Hız Tayini, Hızı Etkileyen Faktörler, Katalizör.
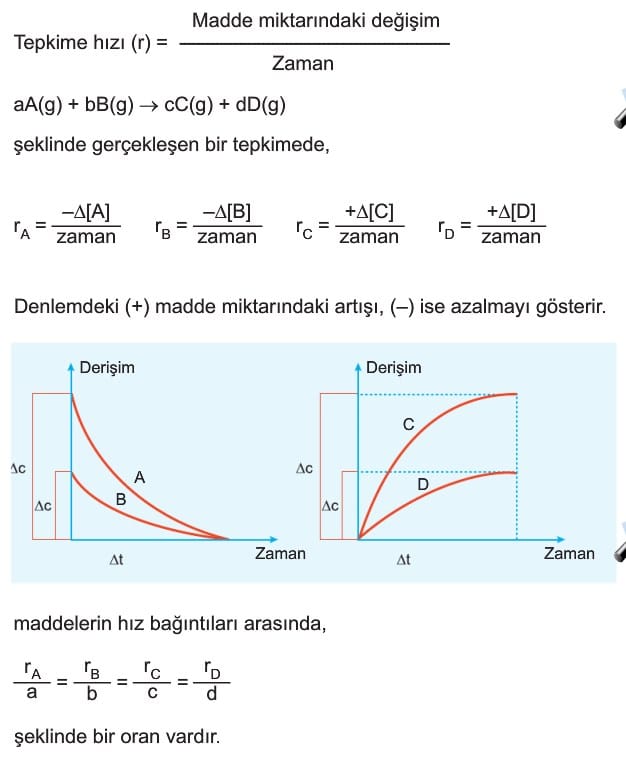
Tepkime Hızları Konu Anlatımı soruları çözümleri 11. sınıf kimya özet
Hız denkleminde yer alan maddenin derişimi arttıkça hız artar Derişim hız sabitini (k) etkilemez. Sayısal yorumlama hız denklemi olmadan ya-pılamaz. [N2] [H2] Tepkime Hızı 2 Kat Sabit Sabit 2 Kat 1/2 Kat 2 Kat 4 kat 1/2 Kat N 2(g) + 3 H 2(g) g 2NH 3(g) tepkimesi için aşağıdaki tabloyu tamamlayalım; 2010 2013 2018 2021 2011

Kimyasal Tepkimelerde Hız Soru Çözümü 1 YouTube
Tepkimelerde Isı Değişim. Kimyasal tepkimeler tanecikler arasındaki bağların kopup, yeni bağların oluşması esasına dayanır. Bağların kopması ve yeni bağların oluşmasında enerji akışı söz konusudur. Tuz, su gibi bileşiklerin elementlerinden elde edilmesi vb. bütün kimyasal tepkimeler enerji olmadan gerçekleşmez.

Hız Denklemi ve Tepkime Derecesi (Kimya) YouTube
#matematik#kimya#biyoloji#geometri#fizik#edebiyat#tarih#rehberlikPDF : https://drive.google.com/file/d/1UYOEsSWwhKBEz4d3G6d_Y8VhYNLE0gM2/view?usp=sharingKANA.

Mavi ders ALİ KARAGÖZ KİMYASAL TEPKİMELERDE ENERJİ
Bu modül, kimyasal tepkimelerde hız kontrolünü, denge kontrolünü ve kimyasal tepkimelerde çözünürlük dengeleri kontrolünü kuralına uygun yapabilme ile ilgili bilgi ve becerilerin kazandırıldığı bir öğrenme materyalidir. SÜRE 40/32 ÖN KOġUL YETERLĠK Kimyasal tepkimelerde hız ve denge kontrolü yapmak MODÜLÜN AMACI